
在肿瘤治疗领域,病毒疗法的研究已跨越百年。自 19 世纪首次受到关注以来,其发展曾因技术壁垒与安全隐患陷入瓶颈,直到近 20 年才迎来突破性进展。如今,病毒在肿瘤治疗中的应用主要分为基因治疗病毒载体和溶瘤病毒(oncolytic viruses, OVs)两大方向,其中经基因修饰的溶瘤病毒,凭借 “精准攻击肿瘤” 的独特优势,成为肿瘤免疫治疗的核心研究热点。
目前,溶瘤病毒已从基础研究走向临床应用,全球批准的溶瘤病毒产品,用于晚期鼻咽癌、黑色素瘤、膀胱癌、胶质母细胞瘤的治疗;给药方式也从单一瘤内注射拓展至膀胱灌注等局部给药模式,为不同肿瘤患者提供了差异化治疗选择。
而随着技术迭代,溶瘤病毒的未来更值得期待:在基因工程领域,科学家正通过 “病毒衣壳改造” 降低预存抗体识别率 —— 例如对腺病毒衣壳蛋白进行定点突变或表面修饰,既保留病毒的肿瘤靶向性,又减少与体内预存抗体的结合,从源头削弱免疫原性干扰;同时,“武装型溶瘤病毒” 研发持续推进,未来的溶瘤腺病毒不仅能直接溶解肿瘤细胞,还可携带更丰富的 “免疫调节基因”(如 PD-1/PD-L1 抑制剂、双特异性抗体基因等),在杀伤肿瘤的同时打破免疫抑制微环境,实现 “溶瘤 + 免疫治疗” 的双重协同效应。
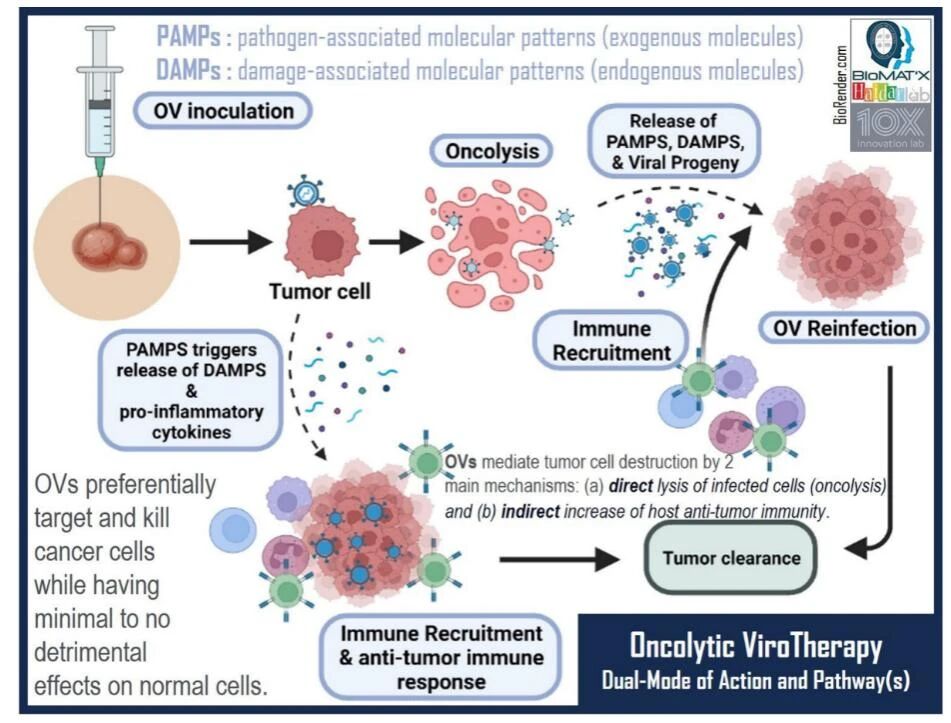
溶瘤病毒疗法的双重作用机制通路:PAMPs 和 DAMPs
图源:《Oncolytic Viruses: From Basics to Challenges to Innovation》
肿瘤治疗的“精准武器”
溶瘤病毒的核心能力,是能选择性感染肿瘤细胞—— 在肿瘤细胞内大量复制,最终 “溶解” 肿瘤细胞,同时对正常细胞几乎无损伤。不仅如此,通过基因工程改造,溶瘤病毒还可携带自杀基因、细胞因子等 “增效模块”,进一步强化溶瘤效果或激活机体抗肿瘤免疫反应。目前,腺病毒、反转录病毒、单纯疱疹病毒等多种病毒已被改造为条件复制型溶瘤病毒,其中溶瘤腺病毒因其高效的肿瘤选择性复制能力、成熟的规模化生产工艺、可装载大片段外源基因的特性,成为当前研究最深入、应用最广泛的溶瘤病毒平台之一。
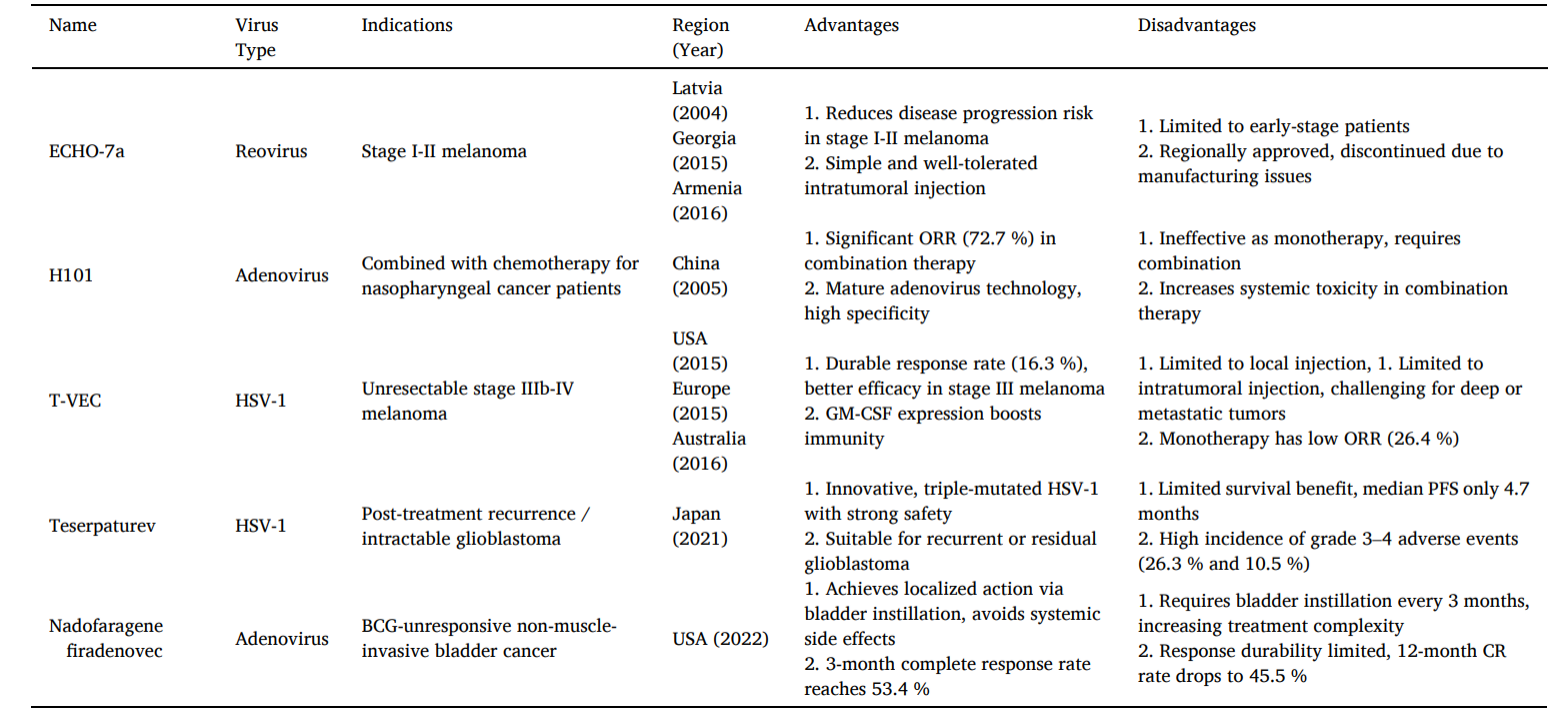
已批准上市OVs产品
来源:《Formulation-optimized oncolytic viruses: Advancing systemic delivery and immune amplification》
溶瘤腺病毒痛点:免疫原性挑战
尽管溶瘤腺病毒优势显著,但其临床应用仍面临一大关键挑战—— 免疫原性。根据 NMPA《溶瘤病毒类药物临床试验设计指导原则(试行)》,溶瘤病毒的中和抗体可能干扰病毒在体内的分布,而机体对病毒的 “预存免疫”(包括体液免疫和细胞免疫)会直接影响给药途径、剂量及次数,因此必须密切监测机体对溶瘤病毒及表达产物的免疫反应。
腺病毒的免疫原性问题尤为突出:作为自然界中最常见的人类病毒之一,5 型人腺病毒在中国人群中的预存抗体阳性率高达 70%~80%。这些预存抗体或治疗后新产生的抗体,可能与溶瘤腺病毒结合,降低病毒的肿瘤靶向性和复制能力,进而削弱治疗效果,甚至导致后续给药失效。
因此,溶瘤腺病毒的免疫原性分析需重点关注三大方向:预存抗体水平、病毒本身的体液 / 细胞免疫反应、病毒表达产物的体液 / 细胞免疫反应。下文将聚焦体液免疫原性分析,详解检测平台与核心方法。
根据 FDA 和 NMPA 的指导原则,抗药抗体(Anti-Drug Antibody, ADA)的检测需遵循 “多层级分析策略”:先通过筛选试验排查所有样本,再对疑似阳性样本进行特异性确证,随后测定阳性样本的抗体滴度,最后检测抗体的中和活性(即中和抗体,Neutralizing Antibody, NAb)。以下分模块解析溶瘤腺病毒及表达产物的体液免疫检测方法。
抗药抗体(ADA)检测
1. 抗药抗体(ADA)检测
ADA 检测的核心是识别样本中针对 “溶瘤腺病毒本身” 或 “病毒表达蛋白” 的抗体,常用酶联免疫吸附法(ELISA)或电化学发光法(ECLIA)。
1.1.针对溶瘤腺病毒的 ADA 检测
采用包被有完整/灭活腺病毒(ADV)的 96 孔板,加入一定稀释倍数的患者血清,使用标记后的病毒衣壳或抗人 IgG 抗体进行检测,通过信号判断抗体是否存在。
由于溶瘤腺病毒的预存抗体率高,单纯判断“阳性 / 阴性” 意义有限,因此通常通过比较给药前后的抗体滴度变化,评估机体是否因治疗产生新的 ADA 或原有抗体水平升高。
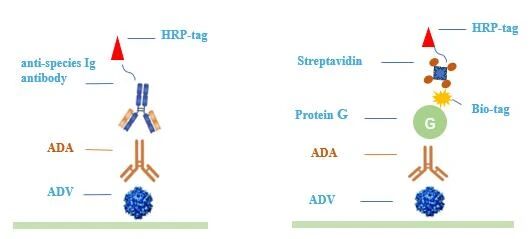
腺病毒的ADA分析示意图
1.2. 针对病毒表达蛋白的 ADA 检测
若溶瘤腺病毒携带外源基因(如 Nadofaragene firadenovec 的 IFN-α 2b 基因),需额外检测针对 “表达蛋白” 的 ADA。此类检测采用桥联检测体系:将 “药物(表达蛋白)” 与 “标记后的药物” 作为捕获试剂和检测试剂,若样本中存在抗表达蛋白的 ADA,可同时结合两种试剂形成 “药物 - ADA - 标记药物” 的桥联复合物,通过 ELISA 或 ECLIA 检测复合物信号。
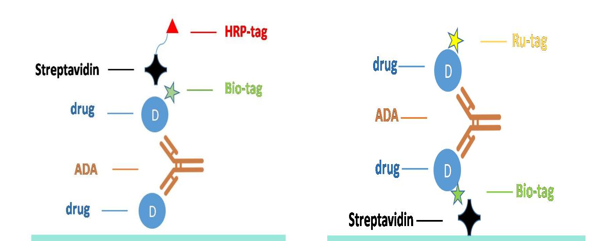
表达蛋白的ADA分析示意图
中和抗体(NAb)检测
NAb 是 ADA 中具有 “功能性” 的子集 —— 可与溶瘤腺病毒或其表达蛋白结合,直接阻断病毒的溶瘤活性或蛋白的生物功能,因此是评估免疫原性对疗效影响的关键指标。NAb 检测需结合药物作用机制(Mechanism of Action, MoA),遵循 “fit-for-purpose” 原则选择方法。
2.1. 针对溶瘤腺病毒的 NAb 检测
溶瘤腺病毒的 NAb 检测主要采用基于细胞的方法,核心是观察抗体是否抑制病毒在靶细胞中的复制或活性,常用三种方法,各有优劣(见下表):
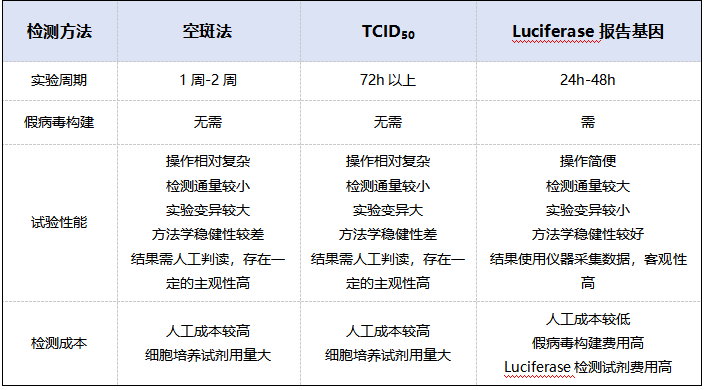
病毒空斑法:将稀释后的病毒与样本血清共孵育后接种细胞,覆盖琼脂糖抑制病毒扩散,培养 1~2 周后染色计数 “病毒空斑”(病毒复制形成的细胞溶解区)。若样本中存在 NAb,空斑数量会减少,通过空斑抑制率判断 NAb 活性。该方法是病毒滴度检测的 “金标准”,但操作复杂、周期长(1~2 周)、通量低,且结果需人工判读,主观性较强。
TCID50 法:TCID50(50% 组织培养感染剂量)是指能使 50% 靶细胞发生感染的病毒剂量。将病毒 - 血清混合物与细胞共孵育 72 小时以上,观察细胞病变效应(CPE),通过统计学方法计算 TCID50 值,若 NAb 存在,TCID50 值会升高。该方法无需构建假病毒,但同样存在操作复杂、变异大、通量低的问题。
Luciferase 报告基因法:先构建携带荧光素酶(Luciferase)基因的重组腺病毒(ADV-luci),将其与样本血清共孵育后感染靶细胞(如 HEK293 细胞)。若样本中存在 NAb,病毒感染会被抑制,荧光素酶表达量降低,通过检测荧光信号强度可量化 NAb 活性。该方法操作简便、周期短(24~48 小时)、通量高,结果客观性强,但需提前构建假病毒,检测试剂成本较高。
此外,细胞活性法(如 MTT 法)、GFP 报告基因法、免疫印迹法等也可用于 NAb 检测,需根据病毒特性、实验室条件综合选择。
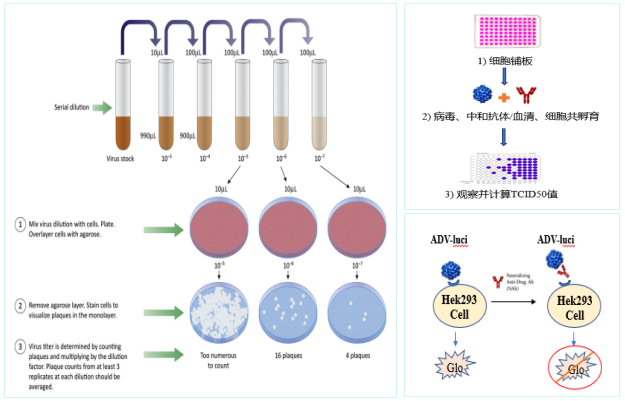
溶瘤腺病毒NAb分析示意图
三种溶瘤腺病毒Nab检测方法比较
2.2 针对病毒表达蛋白的 NAb 检测
与病毒本身的 NAb 检测不同,表达蛋白的 NAb 检测通常采用非细胞方法:将表达蛋白(靶蛋白)与标记后的靶蛋白混合,若样本中存在 NAb,会与两种靶蛋白结合形成复合物,导致游离的标记靶蛋白减少,通过检测游离标记信号的变化,判断 NAb 的中和活性。该方法无需细胞培养,操作更简便,适合高通量检测。
方法学的特殊考量
细胞库管理:基于细胞的检测(如空斑法、TCID50 法)需建立足量的标准化细胞库,细胞复苏后可直接使用或静置培养一段时间,确保细胞状态稳定,避免因细胞活性差异影响检测结果。
阴性对照筛选:由于 5 型人腺病毒在中国人群中的预存抗体率高达 70%~80%,常规筛选 10 例未给药个体难以获得合格的阴性对照。临床实验中通常需筛选 200 例以上人血清,从中挑选抗体阴性样本混合,作为阴性对照。
稀释液选择:在 ADA/NAb 滴度分析中,可比较阴性对照与稀释液(如 PBS)作为稀释基质的信号差异,通常优先选择 PBS 作为稀释液,减少基质干扰。
试剂准备:病毒表达蛋白若为自主制备,需预留足够的制备周期;若购买商用试剂,需提前验证试剂与检测体系的兼容性(如结合活性),确保试剂可用。
未来展望
除了基因工程改造与 “武装化” 设计,溶瘤病毒的未来发展还将在给药技术、联合策略、临床应用范围上实现多维度突破:
在给药技术层面,局部精准给药方案持续优化 —— 针对深部实体瘤的 “影像引导下瘤内注射”“介入导管靶向递送” 等技术,可减少病毒在全身循环中的损耗;“载体包裹递送”(如脂质纳米颗粒包裹病毒)更能直接保护病毒不被血液中的抗体清除,大幅提升药物到达肿瘤部位的效率,解决当前深部肿瘤给药难的问题。
在联合治疗领域,协同策略将成为主流 —— 溶瘤腺病毒与化疗、放疗联合,可通过 “放化疗破坏肿瘤细胞屏障 + 病毒增强溶瘤效应” 提升疗效;与 CAR-T 细胞治疗联合时,病毒溶解肿瘤细胞释放的肿瘤抗原,能为 CAR-T 细胞提供 “靶点信号”,增强其肿瘤杀伤特异性,同时降低单一疗法的剂量依赖性毒性,让治疗更安全、更耐受。
在临床应用拓展上,未来溶瘤腺病毒的适应症将从鼻咽癌、膀胱癌等向肺癌、肝癌、胰腺癌等难治性实体瘤延伸;伴随诊断技术的进步,通过检测患者预存抗体水平、肿瘤微环境特征等生物标志物,可实现 “个体化给药方案” 定制 —— 例如为预存抗体高的患者选择衣壳改造型病毒,为免疫抑制微环境患者选择携带免疫激活基因的病毒,让每一位患者都能获得最适配的治疗方案,真正实现 “精准抗癌” 的终极目标。
参考文献:
1. 《溶瘤病毒类药物临床试验设计指导原则(试行)》 2021.02
2. Immunogenicity Testing of Therapeutic Protein Products - Developing and Validating Assay for Anti-Drug Antibody Detection: Guidance for Industry. FDA, 2019.
3.《药物免疫原性研究技术指导原则》, NMPA, 2021.
4. Wang X , Xing M , Zhang C, et al. Neutralizing antibody responses to enterovirus and adenovirus in healthy adults in China[J]. Emerg Microbes Infect, 2014 May;3(5):e30. doi: 10.1038/emi.2014.30.
5. Viruses. DOI: http://dx.doi.org/10.1016/B978-0-12-803109-4.00004-0.
6. Tissue Culture Infectious Dose (TCID50) Assays | BMG LABTECH.
7. Haidar ZS. Oncolytic Viruses: From Basics to Challenges to Innovation[J]. Innov Discov,2024.1(3):27.
8. Zhou, XL, Hu SF, Wang X. Recent Advances in Oncolytic Virus Combined Immunotherapy in
Tumor Treatment[J]. Genes Dis,2025,12:101599.
9. Ma NY, Gao J, Pang XA , et al. Formulation-optimized oncolytic viruses: Advancing systemic delivery and immune amplification[J]. J Control Release, 2025, 383:113822.
益诺思实验室测试事业部
拥有国际先进的生物分析实验室与规模化细胞房
汇聚经验丰富的专家与技术团队,确保数据精准可靠
恪守NMPA、FDA等全球高标准监管要求
拥有完善的质量管理体系,为药物申报提供坚实保障
提供覆盖药物全研发周期的一站式生物分析服务
能力广泛涵盖小分子、大分子、CGT、小核酸及多特异性抗体等前沿领域
04卓越的CGT项目经验
累计承接80+ 细胞治疗与90+ 基因治疗产品项目
具备深厚的CGT产品实战经验,强力赋能创新药物研发
版权说明:本文内容由益诺思原创,仅用于知识分享及信息交流。读者个人转载需注明文章出处,谢绝媒体(含个人自媒体)或机构未经授权以任何形式转载、摘编、复制或利用其它方式上传至其它平台。
Copyright © 2017-2021©Shanghai InnoStar Bio-tech Co., Ltd. All Rights Reserved. Created By VPABrand.com